اسید نیتریک
اسید نیتریک (HNO3) یکی از اسیدهای قوی و مهم در صنایع شیمیایی است. این اسید از طریق اکسیداسیون آمونیاک با استفاده از هوا در فرآیند Ostwald تولید میشود. اسید نیتریک کاربردهای متعددی دارد؛ یکی از مهمترین آنها تولید نیتراتها است، به ویژه نیترات آمونیوم و نیترات کلسیم، که به عنوان کود در کشاورزی مورد استفاده قرار میگیرند. همچنین، این اسید در ساخت مواد انفجاری مانند تیانتی و نیترات گلیسرین نقش حیاتی دارد. علاوه بر این، اسید نیتریک به عنوان یک ماده اولیه در صنایع داروسازی و تولید قوامدهندهها به کار میرود. با وجود کاربردهای گسترده، باید به خطرات این ماده توجه کرد، زیرا خورنده و سمی است و میتواند آسیبهای جدی به پوست و چشمها وارد کند. لذا رعایت اصول ایمنی هنگام کار با آن الزامی است.
-
 تحویل اکسپرس
تحویل اکسپرس
-
 خدمات آموزشی
خدمات آموزشی
-
 کیفیت بالا
کیفیت بالا
-
 مشاوره فنی
مشاوره فنی
قیمت ( هر کیلوگرم ) : {{ price }} تومان
قیمت ( هر کیلوگرم ) : {{ price }} تومان
قیمت ( هر کیلوگرم ) : {{ price }} تومان
اسید نیتریک (HNO₃) یک اسید قوی و بسیار خورنده است که نقش حیاتی در صنایع شیمیایی و فرآیندهای صنعتی ایفا می کند. این اسید به طور معمول به صورت محلول آبی وجود دارد و می تواند به غلظت های مختلفی از جمله محلول های رقیق و غلیظ دست یابد. به دلیل خواص شیمیایی خاص و توانایی بالای اکسیداسیون، این ماده به طور گسترده ای در تولید نیترات ها، از جمله نیترات آمونیوم و نیترات کلسیم، مورد استفاده قرار می گیرد. این نیترات ها به ویژه در کشاورزی به عنوان کودهای نیتروژنی مورد توجه قرار دارند. علاوه بر کاربردهای کشاورزی، نیتریک اسید به عنوان یک ماده اولیه در تولید مواد انفجاری، مانند تی ان تی و نیترات گلیسرین، شناخته شده است. همچنین این اسید در صنایع داروسازی به عنوان یک واسطه شیمیایی در تولید داروها و ترکیبات فعال به کار می رود. با توجه به این که این اسید یک ماده بسیار خورنده و سمی است، مطالعه و انتخاب صحیح آن ضروری است. برای اطلاعات دقیق تر و جامع تر در مورد این ماده شیمیایی، مطالعه کاتالوگ آن بسیار مهم و ضروری می باشد. این کاتالوگ شامل اطلاعاتی در مورد ویژگی ها، کاربردها، و نکات ایمنی مربوط به این ماده است که می تواند به کاربران کمک کند تا انتخاب بهتری داشته باشند. اگر شما به دنبال مشاوره، خرید، یا اطلاعات بیشتر در مورد اسید نیتریک هستید، می توانید با کارشناسان دلکو صنعت تماس بگیرید. تیم ما آماده است تا به شما در انتخاب مناسب ترین گزینه کمک کند و اطلاعات لازم را در اختیار شما قرار دهد.
فروش اسید نیتریک
اسید نیتریک (HNO₃) یکی از اسیدهای قوی و پرکاربرد در صنایع شیمیایی است که به دلیل خواص خورندگی و اکسیدکنندگی بالا، در تولید انواع محصولات شیمیایی نقش کلیدی دارد. این اسید به طور معمول به صورت محلول آبی و در غلظت های مختلفی از رقیق تا غلیظ در دسترس است. فرآیند تولید آن عمدتاً از طریق اکسیداسیون آمونیاک در حضور اکسیژن و در دماهای بالا انجام می شود. یکی از مهم ترین کاربردهای این اسید تولید نیترات ها است، به ویژه نیترات آمونیوم، که به عنوان کود نیتروژنی در کشاورزی مورد استفاده قرار می گیرد. همچنین، اسید نیتریک در تولید مواد منفجره مانند تی ان تی و نیترات گلیسرین نیز به کار می رود و به عنوان یک عامل اکسیدکننده قوی در بسیاری از واکنش های شیمیایی استفاده می شود. علاوه بر این، در صنایع داروسازی، این اسید به عنوان یک ماده اولیه برای تولید داروها و ترکیبات شیمیایی فعال به کار می رود. در صنایع الکترونیک و ساخت مواد پیشرفته نیز کاربرد دارد. با توجه به خطرات ناشی از مصرف نیتریک اسید، شامل خورندگی و سمی بودن، رعایت اصول ایمنی هنگام کار با این ماده ضروری است. به همین دلیل، آگاهی از اطلاعات فنی و ایمنی این اسید قبل از استفاده، به ویژه از طریق مطالعه کاتالوگ ها و منابع معتبر، بسیار مهم است. در نهایت، این محصول به عنوان یکی از مواد شیمیایی کلیدی در فرآیندهای صنعتی و تحقیقاتی به شمار می آید و توجه ویژه ای به خواص و کاربردهای آن لازم است.

خواص نیتریک اسید
خواص شیمیایی اسید نیتریک (HNO₃) به دلیل ساختار شیمیایی خاص و ویژگی های اکسیدکنندگی آن، بسیار مهم و قابل توجه است. در زیر به برخی از خواص شیمیایی این اسید اشاره می شود:
اکسیدکنندگی: یک اکسیدکننده قوی است که می تواند با بسیاری از فلزات و ترکیبات شیمیایی واکنش دهد. این خاصیت باعث می شود که در تولید مواد منفجره و نیترات ها به کار رود.
واکنش با فلزات: می تواند با فلزات مختلفی مانند آهن، مس و روی واکنش دهد. این واکنش ها معمولاً تولید نمک های نیتراتی و گاز هیدروژن می کند.
H2+ Cu(NO3)2 →2HNO3+ Cu
تجزیه حرارتی: در دماهای بالا تجزیه می شود و نیتروژن دی اکسید (NO₂) و آب تولید می کند.
H2O+ 2NO2 → 2HNO3
واکنش با بازها: با بازها واکنش می دهد و نمک های نیتراتی تولید می کند. به عنوان مثال، واکنش با هیدروکسید سدیم (NaOH) به تولید نیترات سدیم (NaNO₃) و آب می انجامد:
H2O+ NaNO3 → HNO3+ NaOH
واکنش با کربن: این اسید می تواند با کربن یا مواد کربنی دیگر واکنش دهد و نیتروژن و دی اکسید کربن تولید کند.
H2O+ 2NO2+ CO2 → 2HNO3+C
تشکیل نیترو ترکیبات: اسید نیتریک در واکنش های نیتراسیون به کار می رود، جایی که می تواند گروه نیترو (-NO₂) را به ترکیبات آلی اضافه کند. این واکنش در صنایع دارویی و شیمیایی کاربرد دارد این خواص شیمیایی، نقش مهمی در کاربردها و فرآیندهای صنعتی نیتریک اسید دارند و نیاز به آگاهی و احتیاط را هنگام استفاده از این ماده نشان می دهند.
ساختار اسید نیتریک
این اسید از یک اتم هیدروژن، یک اتم نیتروژن و ۳ اتم اکسیژن تشکیل شده است و ساختار مسطح دارد. در حالت ذوب شده نیز از غلظت بالاتری برخوردار بوده و دیاکسید نیتروژن محلول دربردارد. اولین ماده تولید کننده نیتریک اسید، آمونیاک است و از این اسید صنعتی در واکنش های شیمیایی به عنوان یک اکسید کننده و تنظیم محیط اسیدی استفاده می شود.

کاربرد اسید نیتریک
اسید نیتریک به دلیل خواص و ویژگی های شیمیایی واکنش پذیریاش، در بسیاری از صنایع و زمینه های مختلف کاربرد دارد. برخی از کاربردهای مهم این اسید عبارتند از:
تولید کودهای نیتروژن دار: برای تولید کودهای نیتراتی مانند نیترات آمونیوم و نیترات پتاسیم به کار می رود. این کودها به عنوان منابع اصلی نیتروژن برای رشد گیاهان در کشاورزی استفاده می شوند.
صنایع فرآیندی: در صنایعی که به اکسیداسیون و اسیدکاری فلزات نیاز دارند، اسید نیتریک به عنوان یک اکسیدان قوی استفاده می شود. این شامل تمیزکاری فلزات، تولید کاتالیست ها، و تولید انواع مواد شیمیایی مانند نیتروگلیسیرین و TNT می شود.
صنایع پلیمری: در تولید برخی از پلیمرها و رزینهای مصنوعی استفاده می شود. این شامل تولید نایلون و پلی استرها است.
تولید مواد شیمیایی و دارویی: این اسید در سنتز بسیاری از مواد شیمیایی مانند رنگ ها، رزین ها، پلاستیک ها، و داروها مورد استفاده قرار می گیرد.
تولید انرژی: در برخی از سیستم های تولید انرژی مانند سلول های سوختی (Fuel Cells) و موتورهای احتراق داخلی به عنوان یکی از مواد اولیه استفاده می شود.
کاربردهای آزمایشگاهی: به عنوان یک معرف شیمیایی در آزمایشگاه ها برای تجزیه و تحلیل نمونه ها و آزمون های شیمیایی مورد استفاده قرار می گیرد. همچنین، این اسید در بسیاری از صنایع دیگر از جمله صنایع الکترونیک، فلزات، نساجی، و تصفیه آب نیز کاربرد دارد.
کشاورزی: حدود ۸۰ درصد نیتریک اسید در صنعت کشاورزی و به منظور ساخت کودهای نیترات آمونیوم و فسفات های طبیعی استفاده می شود.
صنایع غذایی: از این اسید در صنایع غذایی به منظور تولید پتاسیم و نیترات های سدیم استفاده می شود. سدیم نیتریت با E250 و پتاسیم نیتریک E249 در فرایند پردازش گوشت هایی نظیر کالباس، سوسیس و غیره به عنوان مواد نگهدارنده مورد استفاده قرار می گیرند. زیرا سدیم نیتریت و پتاسیم نیتریک حاوی یون نیتریت هستند و این یون از مسمومیت های غذایی کشنده و رشد باکتری ها در فراورده های گوشتی جلوگیری می کند. همچنین موجب می شود که رنگ گوشت، قرمز و تازه بماند.

استخراج طلا: از این اسید برای جداسازی و همچنین خالص سازی فلزاتی نظیر نقره و طلا نیز استفاده می شود. زیرا قادر است ناخالصی هایی نظیر متا اکسیدها را از سطح طلا و نقره حل کند.
دارویی: در صنعت پزشکی از نوع خالص این اسید به عنوان یک ماده سوز آور جهت درمان زگیل و دیگر بیماری های مشابه استفاده می شود. همچنین برای درمان سوء هاضمه نیز نوع رقیق شده آن مورد استفاده قرار می گیرد.
سوخت موشک: برای تهیه سوخت موشک از اسید نیتریک در اشکال مختلف استفاده می شود.
سایر کاربردها: علاوه بر موارد نام برده این محصول کاربردهای دیگری نیز دارد که شامل موارد زیر هستند.
- قدیمی کردن چوب و چرم
- شستشوی فلزات
- ساخت ترکیبات عالی نیتروژن دار
- ساخت مواد منفجر و تیزاب سلطانی
- تولید پلاستیک و رنگ
- تهیه پلیمرهایی نظیر پلی اورتان و پلی آمیدها
مشخصات فنی نیتریک اسید
اسید نیتریک (HNO₃) یکی از اسیدهای قوی و بسیار مهم در صنایع شیمیایی است که کاربردهای گسترده ای دارد. این ماده به عنوان یک اکسیدکننده قوی و خورنده، در تولید نیترات ها، مواد منفجره، و همچنین در فرآیندهای داروسازی و شیمیایی به کار می رود. این اسید به طور معمول به صورت محلول آبی و در غلظت های مختلف موجود است. این اسید به دلیل خواص شیمیایی خاص و عملکرد مؤثرش در واکنش های شیمیایی، از اهمیت بالایی برخوردار است. شناخت دقیق مشخصات فنی اسید نیتریک برای استفاده ایمن و مؤثر از این ماده ضروری است. در ادامه به بررسی مشخصات فنی این اسید می پردازیم:
| مشخصات | نتایج |
| نام ماده | اسید نیتریک |
| فرمول شیمیایی | HNO3 |
| جرم مولکولی | 63.01 گرم بر مول |
| نقطه دوب | 42- درجه سانتی گراد |
| نقطه جوش | 83 درجه سانتی گراد |
| دانسیته | 1.51 گرم بر سانتیمتر مکعب |
| pH | 1 |
| شکل ظاهری | مایع بی رنگ مایل به زرد خیلی روشن |
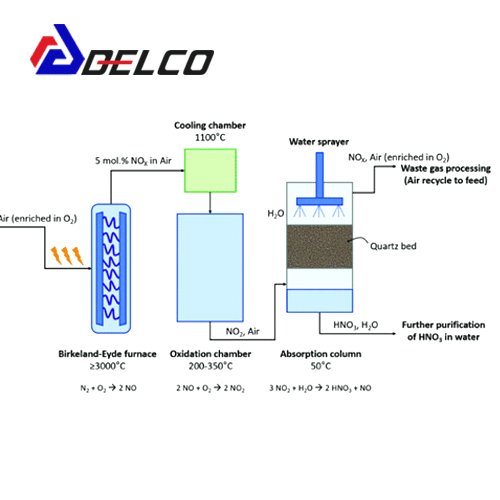
تولید اسید نیتریک
برای تولید اسید نیتریک دی اکسید نیتروژن با آب واکنش داده می شود و در طی این واکنش اکسید نیتریت به دست می آید. بنابراین اگر اکسید نیتریت با اکسیژن هوا اکسید شود، حاصل این واکنش دی اکسید نیتروژن خواهد بود. در حال حاضر برای تولید این اسید از فرایند استوالد استفاده می شود. طی این فرایند در حضور رودیوم یا کاتالیزور گاز پلاتین، در فشار ۹ اتمسفر و دمای بالای ۵۰۰ k، آمونیاک بی آب به اکسید نیتریت تبدیل می شود. آنگاه از طریق واکنش اکسید نیتریت با اکسیژن هوا، دیاکسید نیتروژن به دست می آید و سپس برای تولید ملکول عالی اسید نیتریک و اکسید نیتریک، دیاکسید نیتروژن در آب جذب می شود. در انتها نیز یک گروه نیترو به مولکول عالی نیتریک اسید اضافه می شود تا اسید نیتریک معمولی به دست می آید. به طور کلی واکنش های تولید این اسید به شرح زیر است:
4NH3+5O2->4NO+6H2O
NO+1/2O2->4NO2
3NO2+H2O->2HNO3+NO
خطرات اسید نیتریک
همانطور که در ابتدای مطلب نیز به این نکته اشاره شد، اسید نیتریک یک خورنده و اکسید کننده بسیار قوی است. به همین دلیل غلظت های کم آن در طولانی مدت و همچنین غلظت های بالای آن در کوتاه مدت سلامتی انسان را تحت تاثیر قرار می دهد. استنشاق این ترکیب شیمیایی بسیار خطرناک است و همچنین اگر با چشم انسان تماس پیدا کند منجر به سوزش شدید و حتی نابینایی می شود. خوردن این سم خطرناک خورنده، منجر به سوختگی دهان، گلو و همچنین سوراخ شدن معده و بیهوشی می شود. تماس آن با پوست نیز خطرناک است و در مواقعی که به مقدار زیادی روی پوست بریزد، احتمال مرگ را در پی خواهد داشت. به همین دلیل در حین استفاده از آن باید همواره به نکات ایمنی توجه داشت.

قیمت اسید نیتریک
شرکت دلکو صنعت مفتخر است که به عنوان بزرگترین هایپر صنعت و وارد کننده مواد شیمیایی را به بازار عرضه می نماید. قیمت اسید نیتریک که توسط دلکو صنعت در نظر گرفته شده، مناسب و مقرون به صرفه است شما عزیزان می توانید جهت کسب اطلاعات بیشتر درباره انتخاب گرید مناسب از برندهای مختلف و اطلاع از آخرین قیمت ها با کارشناسان و متخصصان شرکت دلکو صنعت تماس حاصل فرمایید و از مشاوره رایگان بهره مند شوید.
| ردیف | شرح | قیمت (تومان) |
| 1 | قیمت اسید نیتریک | تماس بگیرید |
مشخصات اسید نیتریک
دیدگاه کاربران
قیمت اسید نیتریک
سوالات متداول

![خرید اسید نیتریک [کف قیمت + تضمین کیفیت] خرید اسید نیتریک [کف قیمت + تضمین کیفیت]](https://delcosanat.com/assets/site/images/employee.jpeg)

![فروش اسید کرومیک [انواع کاربرد + مشخصات فنی] فروش اسید کرومیک [انواع کاربرد + مشخصات فنی]](https://delcosanat.com/assets/uploads/product/medium/604chromic-acid.M.jpg)
![خرید اسید فسفریک [کف قیمت + تضمین کیفیت] خرید اسید فسفریک [کف قیمت + تضمین کیفیت]](https://delcosanat.com/assets/uploads/product/medium/169phosphoric-acid.jpg)
![خرید اسید اولئیک [کف قیمت + تضمین کیفیت] خرید اسید اولئیک [کف قیمت + تضمین کیفیت]](https://delcosanat.com/assets/uploads/product/medium/964oleic-acid.jpg)
![خرید اسید سولفونیک [کف قیمت + تضمین کیفیت] خرید اسید سولفونیک [کف قیمت + تضمین کیفیت]](https://delcosanat.com/assets/uploads/product/medium/550sulphonic Acid.jpg)
سلمان زاده
۱۴۰۳/۰۷/۱۱سلام، وقتتون بخیر. یه سوال داشتم درباره اسید نیتریک. میخواستم بدونم برای چه مصارفی بیشتر استفاده میشه و آیا امکانش هست که به صورت عمده سفارش بدیم؟ ممنون میشم اگر راهنمایی کنین.
پاسخ